Все фото с https://postnauka.ru/longreads/154747
Биолог Алексей Москалев о том, почему происходит старение, возможных способах его замедления и чему человек может научиться у животных-долгожителей
В проекте «Жить долго» совместно с Корпоративным университетом Сбербанка рассказываем, можно ли победить старение и продлить активный период жизни.
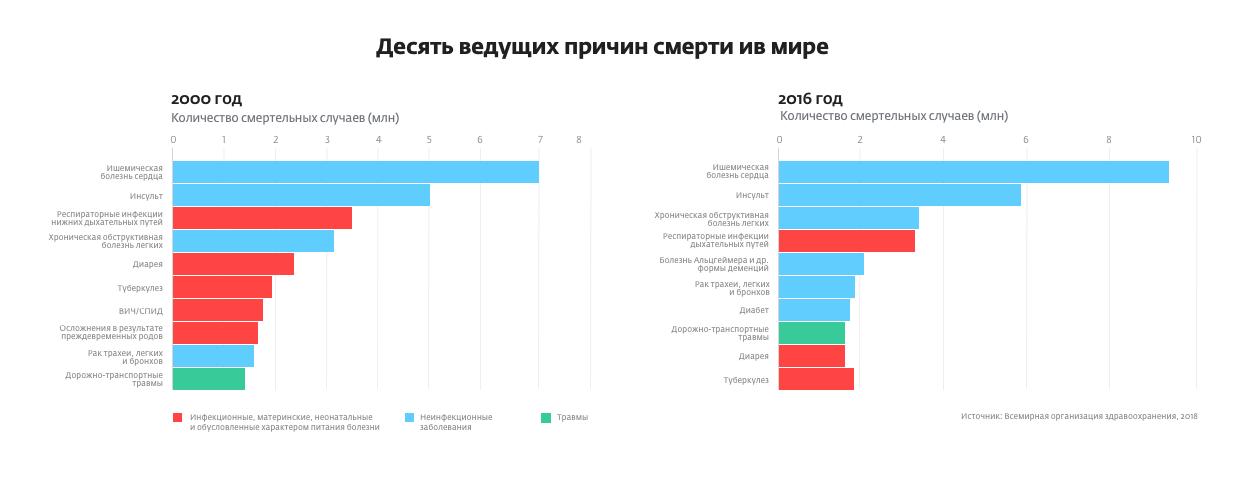
За последние 100 лет средняя продолжительность жизни человека в развитых странах выросла почти вдвое. На это есть объективные причины: уменьшение детской смертности, лечение большинства острых болезней, рост качества жизни, существенное снижение числа смертей по небиологическим причинам, таким как война. Но за последние несколько десятков лет продолжительность жизни увеличилась не так уж сильно, так как человечество исчерпало все простые методы увеличения срока жизни: гигиена, вакцины, антибиотики, здоровый образ жизни. В некоторых странах продолжительность жизни даже уменьшилась, потому что люди начали питаться более дешевой калорийной пищей, что приводит к эпидемиям ожирения. Кроме того, увеличение срока жизни вовсе не гарантирует ее качество. Раньше люди умирали от инфекций в раннем возрасте. Теперь очень многие имеют шанс дожить до глубокой старости.
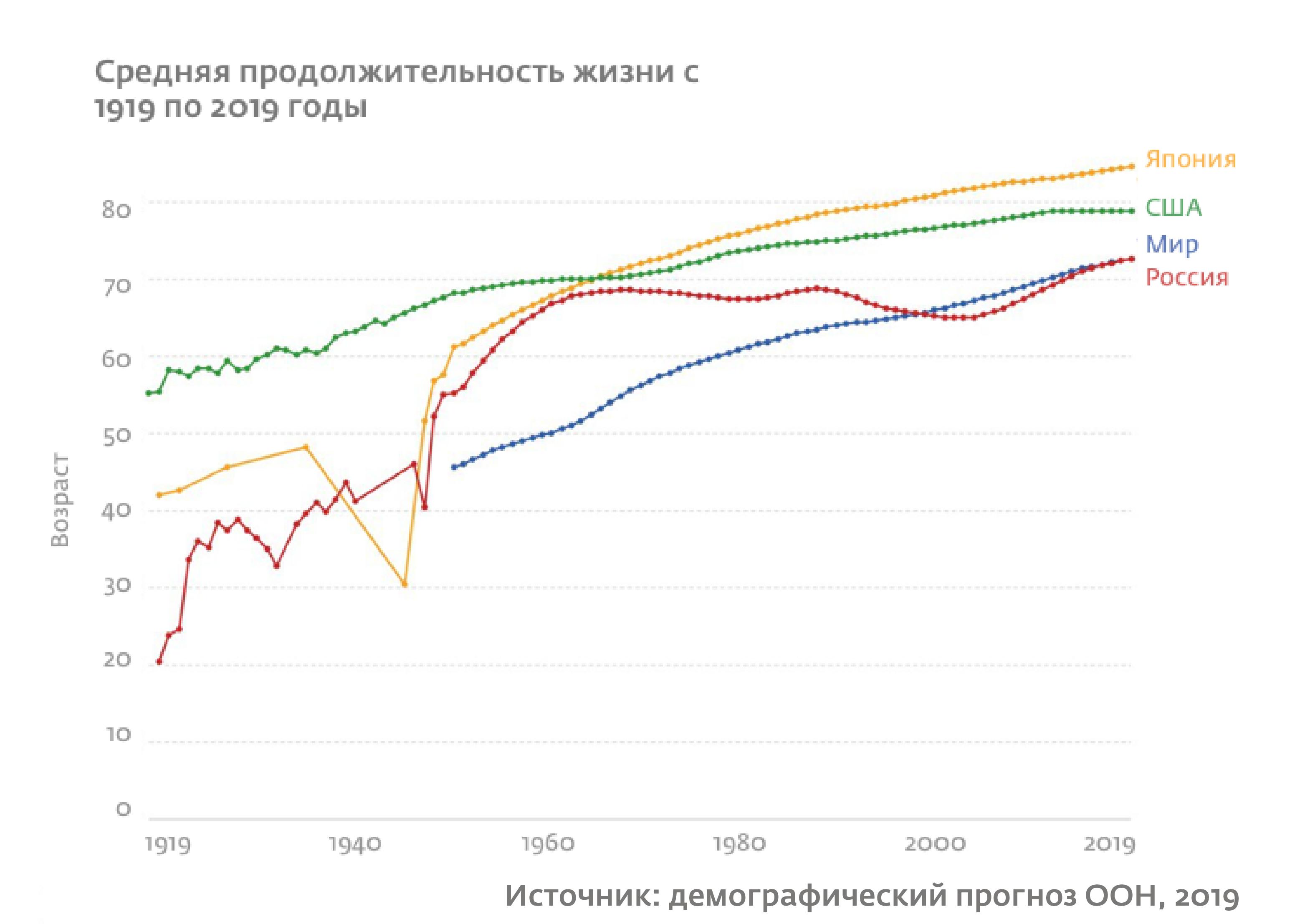
В 2016 году, по сравнению с 2000 годом, в списке причин появляется все больше возрастзависимых заболеваний: к ИБС, инсульту и раку добавились диабет и болезнь Альцгеймера. Источник: данные ВОЗ, 2018
Но жить активной и полной жизнью в этом возрасте смогут далеко не все. По данным Всемирной организации здравоохранения (ВОЗ), среди десяти ведущих причин смертности в настоящее время лидируют возрастзависимые заболевания: ишемическая болезнь сердца (ИБС), инсульт, рак, сахарный диабет. Старение является главным фактором риска для этих и многих других социально значимых хронических заболеваний, включая нейродегенеративные, а именно сосудистую деменцию, болезни Альцгеймера и Паркинсона. В среднем к 50 годам у человека два хронических заболевания, а к 70 годам их уже семь. И если бы эти болезни не были смертельными, человек в глубокой старости приобретал бы весь возможный букет возрастзависимых заболеваний. Поэтому старение можно рассматривать как скрытый, доклинический этап возникновения и протекания этих заболеваний.
Начало старения
Чтобы победить старение и научиться вести полноценную жизнь в пожилом возрасте, необходимо понять, с чем именно мы боремся. И тут нет простого однозначного ответа.
Из оплодотворенной яйцеклетки мы вырастаем в организм, рождаемся и развиваемся, чтобы оставить потомство. Этот процесс физиологического, репродуктивного и психологического созревания индивида называется взрослением. Период оптимальной производительности человека приходится примерно на 20–40 лет: в это время он дает жизнь детям, обеспечивает их выживание, воспитывает их и дает им образование. После этого с точки зрения эволюции мы уже не нужны и можем спокойно умирать.
Есть гипотеза об «эффекте бабушки»: женщины живут дольше, так как отбором им была отведена роль помощи следующему поколению — выращиванию внуков. Кажется, что в этот момент и должно запуститься старение — дегенеративный процесс, приводящий к постепенной утрате адаптационных возможностей и способности поддерживать постоянство параметров внутренней среды.
Согласно исследованиям Кэмбриджского Университета, которое проводили с использованием крыс, старение начинаетя на первых неделях развития плода в утробе матери.
На самом деле старение начинается еще в материнской утробе. Живой организм постоянно «приводит себя в порядок» с помощью специальных ферментативных «наномашин»: они чинят ДНК, утилизируют поврежденные белки, латают клеточные мембраны и так далее. Но со временем ломаются сами механизмы починки. И тогда каскад поломок становится экспоненциальным, и организм получает хронические болезни.
Старение — процесс многоуровневый. Мы утрачиваем сразу множество функций и стареем на всех уровнях: молекулярном, клеточном, тканевом, функциональном, психологическом. Нельзя выделить одну причину или следствие старения. Не существует особых генов, гормонов или органов, нацеленных эволюцией на реализацию программы старения. Старение, как и болезни, является лишь следствием разрегулировки механизмов самоподдержания живой системы и не привносит ничего принципиально нового в организацию нашего тела.
Причины старения
Раньше была популярна идея, что мы живем в окисляющей среде, которая является основным двигателем старения. Согласно этой идее, клетки тела просто не могут не начать накапливать окислительные повреждения, и именно они вызывают различные заболевания, связанные со старением. В конце 1990-х годов многие верили в то, что, если установить защиту против окислительных повреждений и повреждений свободными радикалами (любые молекулы или атомы, содержащие один или несколько неспаренных электронов на внешнем электронном уровне), можно защититься от старения. В магазинах до сих пор продаются пищевые добавки-антиоксиданты. Но в 2000-х годах эту теорию экспериментально проверяли на животных, добавляя антиоксиданты в пищу. Теория оказалась неверной: хотя окисление действительно происходит, оно не играет роли в процессе старения.
Геном — совокупность генов, содержащихся в одинарном наборе хромосом данного организма.
Рассмотрим основные механизмы старения.
Генные мутации. В ходе человеческой жизни сменяется множество поколений клеток организма. Они размножаются посредством деления. В ядрах клеток находятся хромосомы, предназначенные для хранения, реализации и передачи из поколения в поколение генетической программы развития и функционирования организма. Хромосомы состоят из двухцепочечных молекул ДНК. Цепочки ДНК построены из четырех букв (азотистых оснований) по принципу комплементарности: против аденина (A) всегда стоит тимин (T) и наоборот, а против гуанина (G) всегда стоит цитозин (С). Каждый участок ДНК — ген — определяет, как будут строиться белки, выполняющие в организме те или иные функции. В течение жизни некоторые гены случайно или повреждаясь под воздействием внешних неблагоприятных факторов изменяют структуру и активность. Эти изменения в геноме называются мутациями. За долгие годы мутации постепенно накапливаются, что приводит к сбоям в работе организма.
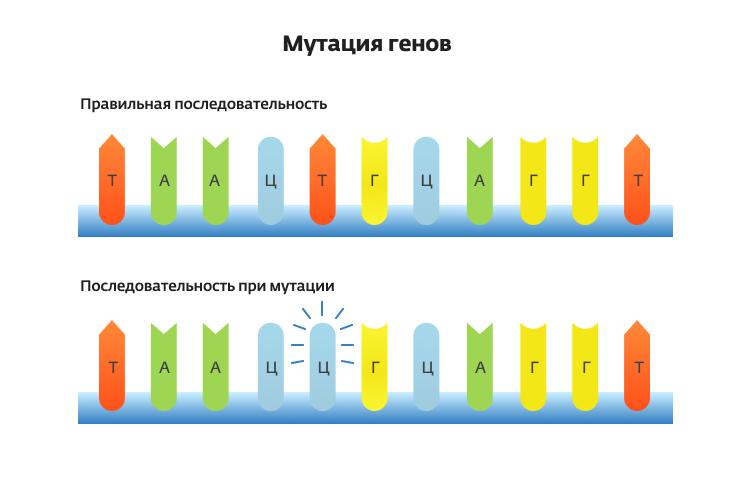
Генные мутации // Максим Мозуль
Но некоторые гены изменяют свою активность, не меняя первичной структуры, — эти изменения называются эпигенетическими. Например, к цитозину — одному из азотистых оснований ДНК — может присоединиться метильная группа, и это будет влиять на выработку того или иного белка в определенный момент времени. Это естественный процесс, благодаря которому клетки печени, например, имеют свой профиль активных генов по сравнению с нейронами головного мозга, несмотря на то что последовательность ДНК всех клеток тела одинаковая. Однако в ответ на стресс, воспаление, при укорочении или повреждении хромосом в процессе деления клеток эпигенетический профиль клетки может меняться, что приводит к возрастному изменению активности генов, в том числе жизненно важных.
Джордж Кристофер Уильямс — американский эволюционный биолог. Профессор биологии Государственного Университета Нью-Йорка.
В 1957 году эволюционный биолог Джордж Кристофер Уильямс предположил, что некоторые гены в разном возрасте дают разный эффект: если в молодом возрасте они чрезвычайно важны для выживания, то в старости только вредят. Например, ген, увеличивающий фиксацию кальция в костях, снижает риск переломов в молодости, но увеличивает риск остеоартрита в старости из-за чрезмерной кальцификации суставов. Эта идея известна как антагонистическая плейотропия.
Укорочение теломер. Когда клетка делится, дочерняя цепь ДНК, образуемая на матрице родительской ДНК, становится несколько короче из-за особенностей работы фермента — ДНК-полимеразы. Дело в том, что ДНК-полимераза не может начать работу с нуля (соединить два свободных нуклеотида). Для нее на самом кончике ДНК специально создается РНК-затравка, к которой она начинает присоединять ДНК-нуклеотиды. Впоследствии РНК-затравка расщепляется, и генетическая информация о кончике хромосомы утрачивается. В череде клеточных делений концы хромосом становятся все более короткими и в определенный момент воспринимаются как повреждение ДНК, которое останавливает деление клетки.
Клетка с поврежденной ДНК в норме не делится, чтобы не переродиться в опухолевую. Это явление неспособности клетки с короткими теломерами делиться носит название клеточного старения. Поэтому на концах хромосом у млекопитающих расположены бессмысленные повторы, образующие теломеры, которые периодически достраиваются ферментом теломеразой. Однако теломераза после рождения выключается во всех клетках, кроме половых и некоторых стволовых. Поэтому с каждым делением клеток теломеры укорачиваются. К концу человеческой жизни они становятся настолько короткими, что каждое последующее деление ставит под угрозу генетическую информацию. Когда это происходит, прекращается деление, например, стволовых клеток и, как следствие, регенерация тканей.
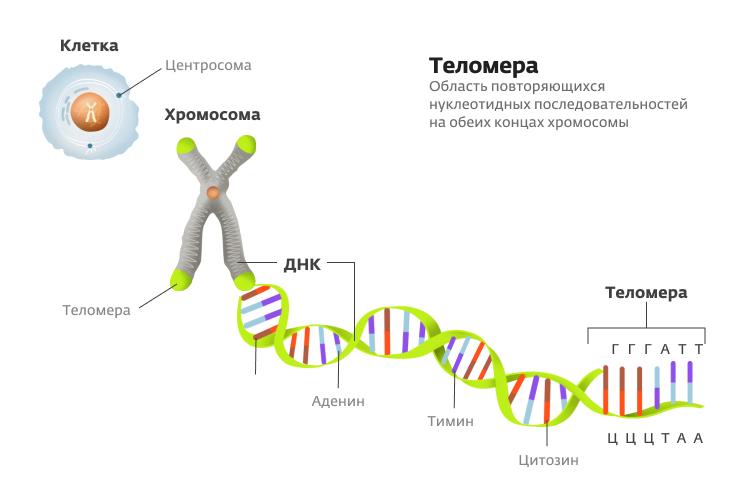
Теломера // Максим Мозуль
Цитоплазма — внутренняя полужидкая среда клетки, в которой расположены ядро и другие элементы мембранного и немембранного строения.
«Затухание» митохондрий. С возрастом утрачивают функцию «энергетические станции» клетки — митохондрии. Это происходит из-за накопления ошибок митохондриальных ДНК и ферментов, ослабления выбраковки поврежденных митохондрий. Перестает хватать энергии для процесса восстановления и роста, что тоже становится одной из причин старения. Кроме того, внутри клетки со временем нарушаются защитные барьеры. Митохондрии перегружаются кальцием и приоткрывают поры временной проницаемости. Через них в клетку выходят кольцевые митохондриальные ДНК, которые в цитоплазме клетки, где их в норме быть не должно, воспринимаются как инфекционное вторжение (некоторые вирусы и бактерии имеют подобные ДНК). Активируется интерфероновый ответ и хроническое воспаление, которое способствует развитию болезней.
Ухудшение качества белков. Со временем происходит нарушение круговорота внутриклеточных белков: поврежденные белки перестают заменяться новыми и накапливаются в организме. А внеклеточные белки, которые практически не обновляются, со временем образуют сшивки. Из-за них ткани становятся жесткими и неэластичными. Отсюда появление морщин, легочной недостаточности, повышенного артериального давления.
В неделящихся клетках (клетки сердечной мышцы, нейроны, которые не заменяются другими в течение почти всей жизни) постепенно скапливаются агрегаты (сгустки) белков, которые нарушают внутриклеточный трафик в цитоплазме, а некоторые из этих клеток довольно протяженные. Белки скапливаются и в эндоплазматической сети — внутренней транспортной и сортировочной системе клетки. Стресс эндоплазматической сети (это похоже на пробку на дороге), в свою очередь, запускает клеточное старение или гибель. Нередко сбиваются в агрегаты и белки вне клеток, бляшки амилоида и тяжи тау-белка в межклеточном пространстве головного мозга связывают с болезнью Альцгеймера — неизлечимой формой возрастной нейродегенерации.
Ослабление биологических барьеров. Ключевую роль для поддержания постоянства параметров внутренней среды играют биологические барьеры, которые находятся в кишечнике, стенке сосудов, коже, между головным мозгом и кровотоком. При старении эти барьеры нарушаются, и через них проникают инфекции, нежелательные молекулы или токсины. Это служит причиной разнообразных болезней: воспалений в стенке желудочно-кишечного тракта, атеросклероза и так далее.
Ночница Брандта — небольшая летучая мышь. Названа в честь немецкого зоолога Иоганна Брандта.
Борьба со старением
Хотя мы знаем о старении довольно много, этого недостаточно, чтобы эффективно и безопасно вмешиваться в эти процессы. Однако некоторые успешные эксперименты поставила сама природа. Так, полярная акула живет 400 лет. А голый землекоп почти не болеет раком, нечувствителен к боли и в неволе доживает до 30 лет, что необычайно долго для грызуна его размеров (13 см): лабораторная мышь живет около трех лет (10 см). По человеку довольно хорошо видно, сколько ему лет, чего не скажешь о голом землекопе: крайне тяжело определить по его внешнему виду, сколько он прожил. Считается, что долголетие землекопа обусловлено активным восстановлением поврежденных оснований ДНК. Более того, есть предположение, что голый землекоп является неотеническим животным — развитие его организма останавливается на стадии новорожденного. А самым удивительным долгожителем считается летучая мышь ночница Брандта: при массе тела всего в 5 грамм она доживает в дикой природе до 40 лет — обычно долго живут те звери, которые имеют наибольшую массу. Ученые расшифровывают геномы животных-долгожителей, что позволяет устанавливать новые генетические причины долголетия.
Джонатан Хатчинсон и Гастингс Гилфорд — британские ученые, хирурги. Впервые описали случай преждевременного старения у шестилетней девочки. Ввели термин «прогерия». Прогерия — редкий генетический дефект, при котором возникают изменения кожи и внутренних органов, которые обусловлены преждевременным старением организма.
Также можно изучать генетику болезней, которые напоминают ускоренное старение человека. Например, при синдроме Хатчинсона — Гилфорда дети доживают примерно до 15 лет: у них выпадают волосы, появляется большое количество морщин, остеопороз. Этот синдром обусловлен мутацией в гене LMNA: из-за нее в клетках накапливается дефективный белок, что приводит к деформации мембран клеточных ядер (где хранятся хромосомы) и сбою многих эпигенетических процессов. Если взять накопление этого белка под контроль, возможно, некоторые дегенеративные процессы удастся замедлить.
В 2009 году Нобелевскую премию по физиологии или медицине присудили Элизабет Блэкбёрн, Кэрол Грейдер и Джеку Шостаку за открытие теломеразы — фермента, способного достраивать теломеры. Доступ к теломеразе имеют только зародышевые и стволовые клетки. Появилась идея, что если дать другим клеткам доступ к активной теломеразе, то они смогут достраивать теломеры, и старение замедлится. Но эта стратегия не сработала. Оказалось, что укорачивание теломер — это барьер для роста раковых опухолей: из-за установления ограничения на количество возможных делений клетки начинающейся опухоли труднее превратиться в по-настоящему злокачественную. Как только клетка получает неограниченный доступ к теломеразе, она начинает неограниченно делиться, и велик риск стать раковой.

Элизабет Блэкбёрн, Джек Шостак и Кэрол Грейдер //
Один из возможных способов продления жизни — редактирование генома. В экспериментах с животными ученые активировали отдельные гены или вносили в них изменения, что иногда приводило к существенному увеличению продолжительности жизни. Эксперименты на мышах показали, что редактирование генома на основе факторов, удлиняющих теломеры или перепрограммирующих обычные клетки в стволовые, способно удлинять жизнь. Банкирование стволовых клеток костного мозга в молодом возрасте с последующим их введением в старости у мышей также способствовало продлению жизни.
На сегодня единого лекарства от старения нет. Даже эксперименты на животных не дают уверенных результатов. Мы знаем, что необходимо комплексное воздействие на различные системы организма, чтобы продлить жизнь и одновременно улучшить ее качество. Можно увеличить устойчивость организма к какому-то стрессу. Можно убрать какие-то повреждения в ДНК. По отдельности эти вмешательства будут малоэффективны, но в совокупности они могут повысить качество жизни. Поэтому нужно систематизировать наши знания о старении, оценить вклад каждого из известных сегодня механизмов старения в долголетие целого организма и создать на этой основе математическую модель старения и долголетия человека. Нужны более точные и безопасные методы редактирования генома человека. Необходимы масштабные клинические исследования фармацевтических препаратов, биодобавок, диет, образа жизни с комплексной оценкой биологического возраста, возрастзависимых заболеваний и смертности от разных причин.
 Алексей Москалев
Алексей Москалевдоктор биологических наук, член-корреспондент РАН, заведующий лабораторией геропротекторных и радиопротекторных технологий Института биологии ФИЦ Коми НЦ УрО РАН, заведующий кафедрой экологии СыктГУ.









